Получение покрытия хим. пас. оксиднофосфатное
Методика анализа раствора химического пассивирования деталей из нержавеющей стали
Определение и назначение.
Настоящая инструкция составлена на основании ОСТ 4 ГО. 054. 076 и предназначена для анализа электролита химического пассивирования деталей из нержавеющей стали (Хим.Пас. оксиднофосфатный раствор).
Состав раствора :
Ангидрид хромовый ГОСТ 2548-77 — 150-200 г/л
Кислота ортофосфорная ГОСТ 6552-80 — 40 – 80 г/л
1.Требования техники безопасности при проведении химических анализов
1.1 Наибольшую опасность при работе представляют:
- токсичность;
- химико-термический ожог;
- электроопасность.
1.2 Источники (носители) опасности:
- электролиты, содержащие концентрированные растворы кислот, используемые при проведении анализов;
- электрооборудование (сушильный шкафы, электронагревательные приборы, контрольно-измерительная аппаратура), находящиеся под напряжением;
- концентрированные растворы кислот и щелочей, используемые при проведении.
1.3 Для обеспечения безопасности работающих необходимо:
1.3.1 Работу с токсичными веществами производить при включенной проточно-вытяжной вентиляции;
1.3.2 Использовать индивидуальные средства защиты (халат, очки, резиновые перчатки);
1.3.3 Убедиться путем внешнего осмотра в исправности защитного заземления и наружной электропроводки;
1.3.4 При выполнении работ пользоваться спец. одеждой.
1.4 При производстве работ соблюдать
«Инструкцию по охране труда для лаборантов хим. лаборатории участка гальваники и очистных сооружений», выполнять требования пожарной безопасности и правил промсанитарии.
2. Оборудование, посуда
2.1 Шкаф вытяжной ШЗНЖ или заводского изготовления.
2.2 Весы аналитические ВЛ-224В ГОСТ Р 53228-2008
2.3 Электроплитка ГОСТ 306-76
2.4 Посуда мерная лабораторная ГОСТ 1770-74
2.5 Колбы конические емкостью 250мл ГОСТ 25336-82
3. Реактивы и материалы
3.1 Соль Мора, 0,1 Н ГОСТ 4208-72
3.2 Кислота ортофосфорная (пл.1,6) ГОСТ 6552-80
3.3 Дифениламин (инд.) ГОСТ 5825-70
3.4 Кислота серная (пл.1,8) ГОСТ 4204-77
3.5 Натрий едкий (0,5 Н р-р) ГОСТ 4328-77
3.6 Метиловый оранжевый (инд. 0,1% раствор) ГОСТ 10816-64
3.7 Фенолфталеин (инд. 0,1% спиртовой раствор) ГОСТ 5850-72
3.8 Спирт этиловый ГОСТ 18300-87
3.9 Калий двухромовокислый 0,1 Н стандарт-титр ТУ 2642-001-56278322-2008
4. Методы анализа
4.1 Определение хромового ангидрида
4.1.1 Сущность метода.
Метод основан на прямом титровании хромового ангидрида солью Мора
4.1.2 Ход анализа.
Отобрать 0,2 мл электролита, разбавить водой до 75-100 мл, добавить 5 мл ортофосфорной кислоты, 4-5 капель дифениламина и титровать полученный раствор 0,1Н раствором соли Мора до перехода синей окраски раствора в зеленую.
4.1.3 Расчет.

- Н— содержание CrO3 (хромового ангидрида), г/л ;
- а — количество 0,1Н раствора соли Мора, пошедшее на титрование, мл;
- в — количество электролита, взятое на анализ, мл ;
- Т— титр 0,1 Н раствора соли Мора (теоретический 0,0033);
- К— поправочный коэффициент к нормальности соли Мора ;
4.1.4 Приготовление растворов.
0,1Н раствор соли Мора готовят следующим образом: 40г соли растворяют в 100 мл воды, приливают 50 мл серной кислоты(1:1), доливают водой до 1л и перемешивают.
4.1.5 Определение поправочного коэффициента к нормальности соли Мора.
Берем 10 мл К2Cr2O7 (калия двухромовокислого) 0,1Н, приливаем 5 мл ортофосфорной кислоты, 4-5 капель дифениламина и титруем 0,1Н раствором соли Мора до перехода синей окраски раствора в зеленую.
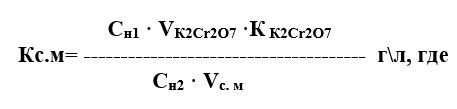
- Сн1— нормальность К2Cr2O7 (0,1Н) ;
- VК2 Cr2O7 – взятый объем K 2Cr 2O7 (10мл) ;
- Vс.м — объем раствора, израсходованного при определении коэффициента, мл ;
- Сн2— нормальность соли Мора (0,1Н); К К2Cr2O7 – 1(стандарт- титр)
4.2 Определение ортофосфорной кислоты.
4.2.1 Сущность метода.
Ортофосфорную кислоту в электролите определяют объемным ацидиметрическим методом.
При расчете вводят поправки на компоненты электролита, реагирующие со щелочью во время титрования.
4.2.2 Ход анализа
Отобрать 0,5 мл электролита в коническую колбу 250 мл, разбавить водой до 100 мл, и титровать 0,5Н раствором едкого натра в присутствии метилового оранжевого (8 капель) до перехода розовой окраски в желтую, после чего добавить 8-10 капель фенолфталеина и продолжать титровать до перехода желтой окраски в розовую.
При определении точки нейтрализации с метиловым оранжевым применяют свидетель- раствор, перетитрованный на 1-2 мл. по метиловому оранжевому.
4.1.3 Расчет.
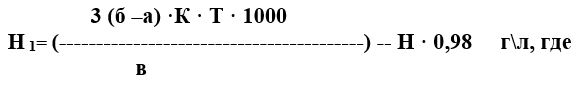
- Н1— содержание ортофосфорной кислоты в растворе, г/л ;
- Н– содержание хромового ангидрида, г/л ;
- б – количество 0,5Н раствора едкого натра, израсходованное на титрование с метиловым оранжевым и фенолфталеином, мл;
- а – количество 0,5Н раствора едкого натра, израсходованное на титрование с метиловы оранжевым, мл;
- Т — титр 0,1Н раствора едкого натра по ортофосфорной кислоте(теоретический титр по ортофосфорной кислоте (0,01635), г/мл;
- K — поправочный коэффициент 0,5Н раствора едкого натра;
- 0,98 – коэффициент пересчета с хромового ангидрида на ортофосфорную кислоту;
- в – количество электролита, взятое на анализ, мл