Методика анализа электролита цинкования
1.Определение и назначение.
Настоящая инструкция предназначена для определения компонентов в ванне цинкования:
1.1 Состав электролита цинкования №1
- Цинк сернокислый – 50 – 120 г/л
- Аммоний хлористый — 200 – 300 г/л
- Кислота борная – 0 — 30 г/л
- Клей столярный костный или клей мездровый — 1 – 2 г/л;
- РН = 5,9-6,5
1.2 Состав электролита цинкования №2
- Цинк сернокислый – 50 – 120 г/л
- Аммоний хлористый — 200 – 220 г/л
- Кислота борная – 0 — 20 г/л
- Блескообразующая добавка ЦКН-3 – 25-40 г/л;
- РН = 4,5-6,3
2. Требования техники безопасности при проведении химических анализов.
2.1Наибольшую опасность представляют:
2.1.1 Повышенное содержание вредных паров в воздухе рабочей зоны.
2.1.2 Обращение с химическими веществами.
2.1.3 Повышенное напряжение в электрической цепи оборудования.
2.1.4 Взрывоопасность
2.1.5 Пожароопасность
2.1.6 Повышенная температура поверхностей нагревательного оборудования.
2.2Источники опасности:
2.2.1 Электролиты, содержащие концентрированные растворы кислот и щелочей
2.2.2 Электрооборудование (контрольно-измерительная аппаратура, сушильные шкафы, электроплитки), находящееся под напряжением;
2.2.3 Растворы кислот, щелочей, солей и органических веществ, используемых при проведении анализов.
2.3. Для обеспечения безопасности работающих необходимо:
2.3.1 Работы с электролитами и концентрированными растворами кислот, щелочей проводить в вытяжном шкафу;
2.3.2. Использовать индивидуальные средства защиты (халат, очки, перчатки)
2.3.3. При производстве работ соблюдать «Инструкцию по охране труда для лаборантов химической лаборатории участка гальваники и очистных сооружений» №7.
3.Оборудование
3.1 Шкаф вытяжной заводского изготовления
3.2 Посуда мерная лабораторная ГОСТ1770 — 74 Е
3.3 Колбы конические емкостью 250мл ГОСТ 1770 -72
3.4 Электроплитка ГОСТ 306 — 76
3.5 Весы аналитические ВЛР –200 ТУ 25- 06 – 383 -68
3.6 Весы лабораторные ГОСТ 24104 – 80
4. Реактивы и материалы
4.1 Трилон Б ГОСТ 10652-73
4.2 Аммиак 25% ГОСТ 3760-79
4.3 Эриохром чёрный Т индикатор ТУ 6-09-1254-64
4.4 Калий хромовокислый 5% раствор ГОСТ 4459 -75
4.5 Серебро азотнокислое 0,1 Н раствор ГОСТ 1277-75
4.6 Кислота серная разбавленная 1:5 ГОСТ 4204-77
4.7 Едкий натр 0,1Н, 0,5Н и 10% растворы ГОСТ4328-77
4.8 Метиловый красный индикатор 0,1% раствор ТУ 6-09-5169-84
4.9 Фенолфталеин индикатор 0,1% р-р, спиртовой ГОСТ 5850-78
4.10 Глицерин разбавленный 1:2 ГОСТ6259-75
4.11 Аммоний хлористый ГОСТ3773-72
5. Методы анализа.
5.1 Определение сернокислого цинка.
5.1.1 Сущность метода
Метод основан на титровании сернокислого цинка трилоном Б в присутствии индикатора эриохрома чёрного Т. Цинк образует с трилоном Б в слабощелочной среде, устойчивый, бесцветный, растворимый в воде комплекс.
5.1.2 Ход анализа
К 5мл электролита прилить 80мл воды, 10мл буферного раствора (см. п. 5.1.4.), добавить 1 крупинку эриохрома чёрного Т и титровать 0,1 Н раствором трилона Б до перехода окраски раствора из винно-красной в синюю.
5.1.3 Расчет:
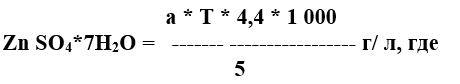
- ZnSO4*7H2O – содержание сернокислого цинка в растворе, г/л
- а – количество 0,1 Н раствора трилона Б, израсходованное на титрование, мл;
- Т – титр 0,1 Н раствора трилона Б по цинку ( теоретический титр 0,00327 ), г/мл;
- 4,4 – коэффициент пересчёта с цинка на сернокислый цинк;
- 5 – количество электролита, взятое на анализ, мл.
5.1.4 Буферный раствор.
54г хлористого аммония растворяют в 200мл воды, приливают 350мл
25% раствора аммиака, доливают водой до 1л и перемешивают.
5.2 Определение хлористого аммония.
5.2.1Сущность метода.
Метод основан на осаждении ионов хлора азотнокислым серебром.
NH4Cl + AgNO3 → AgCl↓ + NH4NO3
В присутствии хромовокислого калия в качестве индикатора, который после связывания всего хлора образует с азотнокислым серебром красноватый осадок хромовокислого серебра.
2AgNO3 + K2CrO4 →AgCrO4↓ + 2KNO3
5.2.2 Ход анализа
К аликвотной части раствора, содержащей 0,5мл электролита, прилить 50мл воды, 2-3мл 5%хромовокислого калия и титровать полученный раствор 0,1Н раствором азотнокислого серебра до появления неисчезающей красноватой окраски раствора.
5.2.3 Расчет:
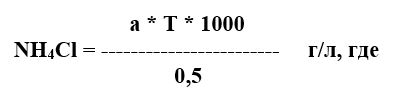
- а – количество 0,1 Н раствора азотнокислого серебра, пошедшее на титрование, мл;
- Т – титр 0,1 Н раствора азотнокислого серебра по хлористому аммонию (теоретический титр 0,00535) г/мл;
- 0,5 — количество электролита, взятое на анализ в мл.
6 Определение борной кислоты.
6.1 Сущность метода.
Хлористый аммоний удаляют кипячением с едким натром, цинк связывают в комплекс с трилоном Б. Борную кислоту с помощью глицерина переводят в более сильную кислоту и титруют щёлочью в присутствии фенолфталеина.
6.2 Ход анализа
В коническую колбу ёмкостью 250мл отбирают 5мл электролита, приливают 50мл воды, 15мл 10% раствора едкого натра и кипятят до полного удаления запаха аммиака. В полученный раствор приливают серную кислоту, разбавленную 1:5, до растворения выпавшего осадка гидрата окиси цинка, затем приливают 0,1 Н раствор трилона Б в количестве равном израсходованному на определение цинка и 1мл его избытка, после этого прибавляют 2-3 капли метилового красного и нейтрализуют 0,5 Н раствором едкого натра, затем 0,1 Н раствором едкого натра до перехода розовой окраски в жёлтую от одной капли едкого натра.
К нейтрализованному раствору добавляют 30мл глицерина, предварительно нейтрализованного по фенолфталеину, несколько капель фенолфталеина и титруют 0,1 Н раствором едкого натра до появления розовой окраски раствора.
Если от прибавления ещё 5мл глицерина не исчезнет окраска, титрование считают законченным.
6.3 Расчет:
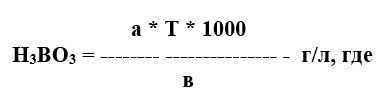
- а – количество 0,1 Н раствора едкого натра, израсходованного на титрование, мл;
- Т – титр 0,1 Н раствора едкого натра по борной кислоте (теоретический титр 0,006183), г/мл.
- в — количество электролита, взятое на анализ, мл.