Электрохимическое оксидирование
Методика анализа электролита
1.Определение и назначение.
Настоящая инструкция составлена на основании ОСТ 4ГО.054.076 и ГОСТ 3765-78 и предназначена для анализа электролита электрохимического оксидирования чёрного следующего состава:
- Аммоний молибденовокислый – 20-22г/л
- Аммоний хлористый – 18-22г/л
- РН = 5,7-6,3
2. Требования техники безопасности при проведении химических анализов.
2.1 Наибольшую опасность представляют:
2.1.1 Токсичность.
2.1.2 Химико-термический ожог.
2.1.3 Электроопасность
2.2 Источники опасности:
2.2.1 Электрооборудование (сушильный шкаф, электроплитка), находящиеся под напряжением.
2.2.2 Концентрированные кислоты и щелочи, используемые при анализе.
2.3. Для обеспечения безопасности работающих необходимо:
2.3.1 Работы с концентрированными растворами кислот, щелочей проводить в вытяжном шкафу.
2.3.2. Использовать индивидуальные средства защиты (халат, очки, перчатки).
2.3.3 Убедиться путём внешнего осмотра в исправности защитного заземления и наружной электропроводки.
2.3.4. При производстве работ соблюдать «Инструкцию по охране труда для лаборантов химической лаборатории участка гальваники и очистных сооружений».
3.Оборудование
3.1 Шкаф вытяжной заводского изготовления
3.2 Посуда мерная лабораторная ГОСТ1770 — 74 Е
3.3 Колбы конические емкостью 250мл ГОСТ 1770 -72
3.4 Электроплитка ГОСТ 306 — 76
3.5 Весы аналитические ВЛА –200-М ТУ 25- 06 – 383 -68
4. Реактивы и материалы
4.1 Трилон Б 0,05 М, раствор готовят по ГОСТ 10398-76 ГОСТ 10652-73
4.2 Аммоний ванадиевокислый ГОСТ 9336-75, 0,05Мр-р
4.3 Аммоний уксуснокислый ГОСТ 3117-78
4.4 Вода дистилированная ГОСТ 6709-72
4.5 Глицерин ГОСТ 6259-75
4.6 Дифенилкарбазон 0,2% спиртовой раствор
4.7 Кислота уксусная ГОСТ 61-75
4.8 Натр гидроокись ГОСТ 4328-77, 20%р-р
4.9 Спирт этиловый ГОСТ 18300 -87
4.10.Фенолфталеин (индикатор) ГОСТ 5850-72, 1% спиртовой р-р
4.11.Метиленовый голубой (индикатор) 0,01% раствор
4.12.Буферный раствор рН 5,2-5,6
Готовят следующим образом:
500г уксуснокислого аммония растворяют в 700мл воды, прибавляют 350мл уксусной кислоты и 80мл глицерина, доводят объём раствора водой до 1500мл и перемешивают.
4.13.Комплексонат ванадия 0,025 М раствор
Готовят следующим образом:
50мл точно 0,05 М раствора ванадиевокислого аммония смешивают с 50 мл точно 0,05 М раствора трилона Б.
4.14.Калий двухромовокислый 5% раствор ГОСТ 4459-75
4.15.Серебро азотнокислое 0,1Н раствор ГОСТ 1277-75
5. Методы анализа.
5.1 Определение хлористого аммония.
5.1.1 Сущность метода
Метод основан на осаждении ионов хлора азотнокислым серебром:
NH4Cl + AgNO3 = AgCl + NH4NO3
В присутствии хромовокислого калия в качестве индикатора, который после связывания всего хлора образует с азотнокислым серебром красноватый осадок хромовокислого серебра.
AgNO3 + K2CrO4 = Ag2CrO4 + 2KNO3
5.1.2 Ход анализа
В коническую колбу ёмкостью 250мл отобрать 5мл электролита, прилить 30мл воды, 2-3мл 5% раствора хромовокислого калия и титруют полученный раствор 0,1 Н раствором азотнокислого серебра до появления неисчезающей красноватой окраски раствора.
5.1.3 Расчет:

- а – содержание 0,1 Н раствора азотнокислого серебра, пошедшее на титрование;
- Т – титр 0,1 Н раствора азотнокислого серебра по хлористому аммонию (теоретический титр 0,00535), г/мл;
- 5 – количество электролита, взятое на анализ, мл.
5.2. Определение молибденовокислого аммония.
5.2.1Сущность метода.
Метод основан на титровании молибденовокислого аммония трилоном Б в присутствии индикаторов
5.2.2 Ход анализа
В коническую колбу ёмкостью 250мл отобрать 10мл электролита, прилить 50мл воды, 2-3 капли раствора фенолфталеина и при перемешивании раствор гидроокиси натрия до слабощелочной реакции. К полученному раствору прибавляют при перемешивании 25мл спирта, 5мл буферного раствора, 1мл раствора метиленового голубого, 1мл раствора дифенилкарбазона. Раствор титруют раствором трилона Б до исчезновения фиолетовой окраски, затем прибавляют 1мл раствора комплексоната ванадия (раствор вновь окрашивается в фиолетовый цвет) и продолжают титровать раствором трилона Б до полного перехода фиолетовой окраски раствора в голубую.
5.2.3 Расчет:
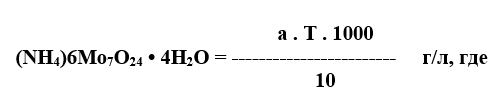
- а – объём точно 0,05 М раствора трилона Б, израсходованный на титрование, мл;
- Т – титр 0,05 М раствора трилона Б по молибденовокислому аммонию (теоритический титр 0,01765), г/мл.
- 10 – количества электролита, взятое для анализа, мл.