Методика анализа раствора для травления цветных металлов
1.Определение и назначение.
Настоящая инструкция предназначена для определения компонентов раствора в ванне травления цветных металлов следующего состава:
- Серная кислота – 750-850 г/л
- Азотная кислота — 50-100 г/л
- Соляная кислота – 1-5 г/л
2. Требования техники безопасности при проведении химических анализов.
2.1 Наибольшую опасность представляют:
2.1.1 Повышенное содержание вредных паров в воздухе рабочей зоны.
2.1.2 Обращение с химическими веществами.
2.1.3 Повышенное напряжение в электрической цепи оборудования.
2.1.4 Взрывоопасность
2.1.5 Пожароопасность
2.1.6 Повышенная температура поверхностей нагревательного оборудования.
2.2 Источники опасности:
2.2.1 Электролиты, содержащие концентрированные растворы кислот и щелочей
2.2.2 Электрооборудование (контрольно-измерительная аппаратура, сушильные шкафы, электроплитки), находящееся под напряжением;
2.2.3 Растворы кислот, щелочей, солей и органических веществ, используемых при проведении анализов.
2.3. Для обеспечения безопасности работающих необходимо:
2.3.1 Работы с электролитами и концентрированными растворами кислот, щелочей проводить в вытяжном шкафу;
2.3.2. Использовать индивидуальные средства защиты (халат, очки, перчатки)
2.3.3. При производстве работ соблюдать «Инструкцию по охране труда для лаборантов химической лаборатории участка гальваники и очистных сооружений».
3.Оборудование
3.1 Шкаф вытяжной заводского изготовления
3.2 Посуда мерная лабораторная ГОСТ1770 — 74 Е
3.3 Колбы конические емкостью ГОСТ 10394 -72
3.4 Весы аналитические ВЛР –200 ТУ 25- 06 – 383 -68
4. Реактивы и материалы
4.1 Аммиак водный, 25% раствор ГОСТ 3760-79
4.2 Барий хлористый, 0,1Н раствор ТУ 6-09-2548-72
4.3 Кислота соляная 0,5Н раствор ГОСТ 3118-77
4.4 Серебро азотнокислое, 0,1Н раствор ГОСТ 1277-75
4.5 Эриохром чёрный Т индикатор ТУ 6-09-1254-64
4.6 Трилон Б 0,1Н раствор ГОСТ 10652-73
4.7 Цинк хлористый 0,1Н раствор ГОСТ 4529-78
4.8 Едкий натр 0,1Н раствор ТУ 6-09-2585-72
4.9 Едкий натр 0,5Н раствор ГОСТ 4328-77
4.10 Фенолфталеин индикатор 1% раствор (спиртовой) ГОСТ 5850-78 4.11 Калий хромовокислый 5% раствор ГОСТ 4459-75
5. Методы анализа.
5.1 Определение серной кислоты.
5.1.1 Сущность метода
Метод основан на титровании сульфат ионов хлористым барием в присутствии индикатора ализарина S.
5.1.2 Ход анализа
Отобрать в мерную колбу ёмкостью 100мл 5мл электролита.Из неё в коническую колбу отобрать 2мл, прилить 10мл дистиллированной воды, 5-7 капель ализарина красного S и нейтрализовать 25% раствором аммиака до фиолетового цвета (рН=2,3-3,7). Снять окраску 0,5Н раствором соляной кислоты до жёлтой, прилить 10мл спирта и титровать 0,1Н раствором хлористого бария до розовой окраски раствора
5.1.3 Расчет:
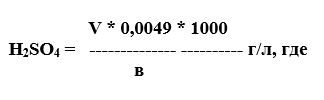
- V – объём 0,1Н раствора ВаСl2*2Н2О, пошедший на титрование, мл
- 0,0049 – количество серной кислоты, соответствующее 1мл 0,1Н раствора хлористого бария;
- в – количество электролита взятого на анализ, мл.
5.2 Определение азотной кислоты.
5.2.1 Сущность метода.
Метод основан на титровании кислоты щёлочью в присутствии фенолфталеина.
5.2.2 Ход анализа
Из раствора в мерной колбе на 100мл, приготовленного для определения серной кислоты, отбирают аликвотную часть 2мл, содержащую 0,1мл. К раствору приливают 150мл воды, 5-7 капель фенолфталеина и титруют 0,1Н раствором щёлочи до появления розовой окраски раствора, не исчезающей в течении 1мин.
5.2.3 Расчет: Расчёт общей кислотности в пересчёте на азотную кислоту

- А – общая кислотность электролита в пересчёте на азотную кислоту, г/л;
- а – количество 0,1Н раствора щёлочи, пошедшее на титрование, мл;
- 0,0063 – титр точно 0,1Н раствора щёлочи по азотной кислоте;
- м – количество электролита, взятое на анализ, мл;
Расчёт количества азотной кислоты
Н = А – (Б * 1,28 + В * 1,72) г/л, где
- А – общая кислотность электролита в пересчёте на азотную кислоту, г/л;
- Н – содержание азотной кислоты, г/л;
- Б – количество серной кислоты, г/л;
- 1,28 – коэффициент пересчёта с серной кислоты на азотную;
- В – количество соляной кислоты, г/л;
- 1,72 – коэффициент пересчёта с соляной кислоты на азотную.
5.3 Определение соляной кислоты
5.3.1 Сущность метода.
Метод основан на осаждении ионов хлора азотнокислым серебром в присутствии индикатора хромовокислого калия:
HCl +AgNO3 = AgCl↓ + HNO3
После связывания всего хлора индикатор образует с азотнокислым серебром красноватый осадок хромовокислого серебра:
2AgNO3 + K2CrO4 = Ag2CrO4↓ + 2KNO3
5.3.2 Ход анализа
2 мл электролита отбирают в коническую колбу ёмкостью 250мл, добавляют 50мл воды. Полученный раствор нейтрализуют 0,5Н раствором едкого натра в присутствии фенолфталеина до слабощелочной реакции. Затем приливают 2мл 5% раствора хромовокислого калия и титруют 0,1Н раствором азотнокислого серебра до появления неисчезающей красноватой окраски – осадка хромовокислого серебра.
5.3.3 Расчет:

- Н — содержание соляной кислоты, г/л;
- а – количество 0,1Н раствора азотнокислого серебра, израсходованного на титрование, мл;
- m – количество электролита, взятое на анализ, мл;
- 0,00365 – титр точно 0,1Н раствора азотнокислого серебра по соляной кислоте.