Методика анализа раствора химической пассивации
Деталей из нержавеющей стали
Определение и назначение.
Настоящая инструкция составлена на основании ОСТ4ГО.054.076 и предназначена для анализа электролита пассивации нержавеющей стали
Состав раствора
Двухромовокислый натрий 20-25 г/ л ГОСТ 4237-76
Кислота азотная 280-500 г/л ГОСТ 4461-67
1. Требования техники безопасности при проведении химических анализов
1.1 Наибольшую опасность при работе представляют:
- токсичность;
- химико-термический ожог;
- электроопасность;
1.2 Источники (носители) опасности:
растворы и электролиты, содержащие свободные кислоты, щелочи, используемые при проведении анализов
электрооборудование(контрольно-измерительная аппаратура, сушильные шкафы, электронагревательные приборы), находящиеся под напряжением.
концентрированные растворы кислот и щелочей, используемые при проведении анализов.
1.3 Для обеспечения безопасности работающих необходимо:
1.3.1 Работу с токсичными веществами производить при включенной приточно-вытяжной вентиляции.
1.3.2 Использовать индивидуальные средства защиты (халат, очки, резиновые перчатки);
1.3.3 При проявлении запаха горького миндаля сообщить начальнику лаборатории.
1.3.4 Убедиться путем внешнего осмотра в исправности защитного заземления и наружной электропроводки;
1.3.5. Пользоваться спец. одеждой;
1.4 При производстве работ соблюдать «Инструкцию по охране труда для лаборантов хим. лаборатории участка гальваники и очистных сооружений», выполнять требования пожарной безопасности и правил промсанитарии.
2. Оборудование, посуда, реактивы.
2.1. Шкаф вытяжной ШЗНЖ или заводского изготовления.
2.2. Весы аналитические ВЛА-200М ГОСТ 24104-01
2.3. Посуда мерная лабораторная ГОСТ 1770-74
2.4. Колбы конические емкостью 250мл ГОСТ 1770-74
2.5. Химические стаканы с носиком емкостью 200-300мл ГОСТ 25336-82
2.6. Соль Мора ,0.1 н ГОСТ 4208-72
2.7. Кислота серная, 1:5 ГОСТ 4204-77
2.8. Перманганат калия, 0,1н ГОСТ 4220-75
2.9 Гидроксид натрия, 0.2 н ГОСТ 4328-77
2.10. Метиловый оранжевый, 0,1%-ный водный раствор ГОСТ 4919.1-77
3. Методы анализа
3.1. Определение двухромовокислого натрия
3.1.1. Сущность метода.
Метод основан на восстановлении шестивалентного хрома до трехвалентного раствором закисной соли железа по реакции:
Na 2 Cr 2O7 + 6FeSO4 +7 H2 SO4 = Cr2 (SO4 )3 +3 Fe2( SO 4)3 +Na2 SO4 + 7 H2 O
Избыток закисной соли железа титруют перманганатом калия:
10FeSO4 +2 KMnO4 + 8H2 SO4 = 5Fe2 ( SO4 )3 +2 MnSO4 + K2 SO4 + 8 H2 O
3.1.2. Ход анализа.
В коническую колбу на 250 мл помещают 3мл анализируемого раствора. Приливают 150 мл воды, 15 мл серной кислоты ,разбавленной 1:5 и 25-30 мл соли Мора. Раствор должен быть зеленым,что свидетельствует о полном восстановлении шестивалентного хрома до трех-валентного.
Избыток соли Мора титруют 0.1 н. раствором марганцовокислого калия до появления слабо-розовой окраски раствора.
3.1.3. Расчет.
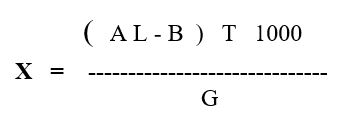
Содержание двухромовокислого натрия в растворе рассчитывают по формуле:
- Х – содержание двухромовокислого натрия в растворе , г/л
- А – количество 0.1 н соли Мора ,добавленное к пробе при определении, мл
- L — соотношение между растворами марганцовокислого калия и соли Мора
- B – объем 0,1н марганцовокислого калия, израсходованное на титрование избытка соли Мора, мл
- Т – титр 0.1 н раствора марганцовокислого калия по двухромовокислому натрию ( теоритический титр 0,00497 ), г/мл
- G – количество раствора , взятое на анализ , мл
3.2. Определение азотной кислоты.
3.2.1Сущность метода
Метод основан на титровании азотной кислоты и хрома раствором едкого натра в присутствии индикатора метилового оранжевого.
3.2.2.Ход анализа.
В коническую колбу на 250 мл отобрать 1 мл анализируемого раствора. Добавить 100мл воды, 3-4 капли метилового оранжевого и титровать раствором едкого натра 0,2н до перехода розовой окраски в желтую.
3.2.3.Расчет
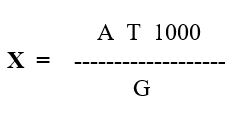
Х – содержание азотной кислоты в растворе, г/л
A – количество 0,2н раствора едкого натра израсходованного на титрование в мл;
Т — титр 0,2н раствора едкого натра по азотной кислоте (теоритический титр 0,012604 ), г/мл
G – объем раствора , взятый на анализ, мл